慢性炎症与衰老
Chronic Inflammation and Aging
生老病死是一个自然过程,衰老也是一样,它与免疫系统对环境的调适与重塑有关。
衰老的过程就是慢性炎症的过程。通俗地讲就是机体为适应环境的变化,如环境中病原微生物的入侵,或是自身代谢产物的作用,而发生的对应反应。对应反应分为促炎症反应和抗炎症反应。这个过程对人体最为有利的形式是促炎症与抗炎症反应的平衡,也称之为健康的衰老。
不健康的衰老是以促炎症反应为主,是指机体的抗炎症反应减弱,而促炎症反应增强,二者的失衡最终导致慢性低烈度炎症,并由此引发一系列与慢性炎症有关的疾病。因此,有西方学者专门为这一现象创造了一个新的名词——炎症性衰老(inflammaging), inflammation是炎症,aging是衰老,组合后就是inflammaging.
现在普遍存在一个现象,看上去健康的老年人,其实各个器官与系统中的促炎症因子与抗炎症因子已出现失衡,表现为血液循环中的促炎症因子水平升高。动物实验结果也表明,高龄鼠类(相当于人类70-75岁年龄)尽管它的各种生理机能,各种活动都很正常,但其冠状动脉中炎症因子的表达已出现失衡现象,促炎症反应处于主导地位。而这种现象就是慢性低烈度炎症的典型表现。
促炎症因子水平的升高,使得原本平衡稳定的血管内环境发生相应的病理性变化,如血管在促炎症因子水平升高后,会变得更易于血液凝集,更易于发生氧化应激反应,并不断放大血管损伤性反应,促进缺血性心脏病的发生发展。
通俗地说,人体原本对轻微的血管损伤有及时自我修复的能力,如果有慢性炎症存在,损伤不但不能及时修复,还会因为炎症造成损伤越来越严重,即放大慢性炎症对血管的损伤,最后引起血管内皮衰老,引发动脉粥样硬化、高血压等疾病的发生。这一系列的病理过程,都是由于炎症因子诱导血管内皮细胞的衰老引起的。这一过程就是我们常说的“内皮性衰老”和“血管衰老”。
需要注意的是,所谓的内皮性衰老,并不意味着内皮细胞自身潜能出现了问题,而是在炎症因子的作用下,内皮细胞的功能发生了改变(功能障碍)。内皮细胞如此,生发内皮细胞的干细胞亦如此。
比如,百岁老人的干细胞在适宜的细胞因子和生长因子的环境下,其生成子细胞的能力与年轻人没有区别,表明老年人干细胞的潜能是完好的,只是由于其周围环境中细胞因子的改变,才导致了老年人干细胞的各种潜能出现明显的衰退。
类似的情况也发生在动物身上。如果将高龄老鼠的祖细胞置于年轻老鼠的血清中进行培养,这些祖细胞立即就恢复了活力;相反,如果将年轻老鼠的祖细胞放置在高龄老鼠的血清中进行培养,这些原本充满活性的祖细胞就失去了原有的活性。这表明,与衰老有关的干细胞活性的下降,主要受到了环境因素的影响,特别是与炎症性衰老有关的细胞因子的影响。
炎症因子(主要是白介素1α)调节内皮细胞衰老的证据也可以在临床上得到验证:比如,做心脏搭桥手术,把切下来的有动脉粥样硬化的冠状动脉拿去做化验,可以看到里面的白介素1水平很高,这说明衰老的内皮细胞出现在冠状动脉硬化斑块表面,这些内皮细胞产生大量的白介素1. 而白介素1能够引起多种不良反应,如抑制内皮细胞增殖、诱导白细胞粘附以及促进血栓形成等。
百岁老人的炎症性衰老总是伴随着抗炎症性衰老的反应,在这种情况底下,即使发生了外源性的感染,也不至于对外缘性的微生物没有一点抵抗能力,而是恰到好处的、及时的完成了一个炎症过程,又恢复到原来的水平,促炎症与抗炎症反应的平衡是他们能够获得健康的衰老过程以及长寿的根本原因。换句话说,对他们而言,不管炎症标记物是否随着年龄的增加而增加(炎症性衰老),只要抗炎症反应仍然完好(抗炎症性衰老),最终的结果就是:基于炎症的疾病将不会发生,或推迟发生,或即使发生了也不会太过严重。
衰老的一个常见症状是肌肉减少症(sarcopenia),表现为无力或是虚弱 (frailty),其本质也是炎症反应。实验表明,正是炎症因子(如肿瘤坏死因子)在肌肉中的高表达,引起肌纤维的凋亡,最终导致肌纤维的减少及肌肉的萎缩。通过抑制炎症因子,就可以最大限度的抑制肌肉萎缩及由此引起的虚弱。由此,可否将这一现象拓展到其他器官?比如心脏、胃和各种腺体,因为衰老是全方位的衰老,而不是单一器官的衰老,答案是:完全可以!
下面这张图展示了衰老的过程:
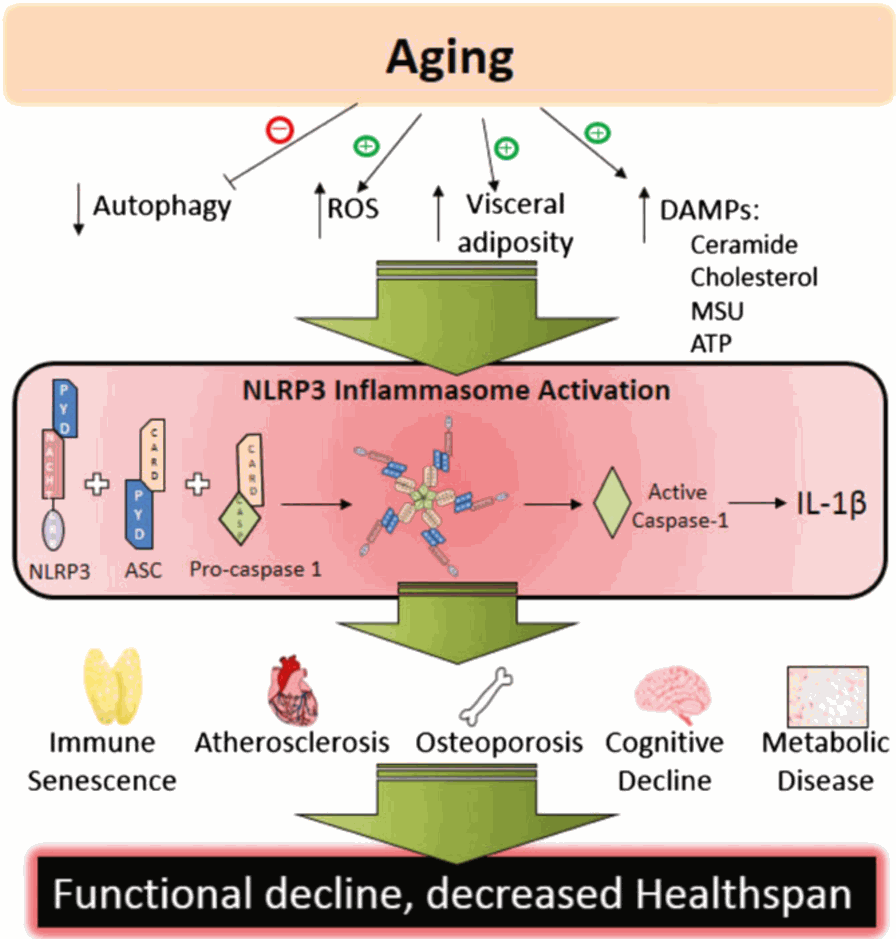
上面白色部分代表衰老过程中各种炎症因子水平上升,当中红色部分表示炎症因子导致炎症小体的激活,即激活了炎症,这些炎症小体会释放白介素1,最后导致下方展示的免疫衰老、动脉粥样硬化、骨质疏松、认知障碍、代谢障碍等病症,最终导致各项功能降低和健康水平的下降。
还有一张图展示了人生的整个过程:

从胎儿状态到进入坟墓,我们可以看到老年的标志是拄拐杖、坐轮椅,这是因为慢性炎症导致肌肉肌腱发生凋亡和萎缩以及其他器官的衰竭,造成了弯腰驼背、坐轮椅,甚至让我们丧失生活的自理能力。
最后这张图是正常人的大腿肌肉示意图:
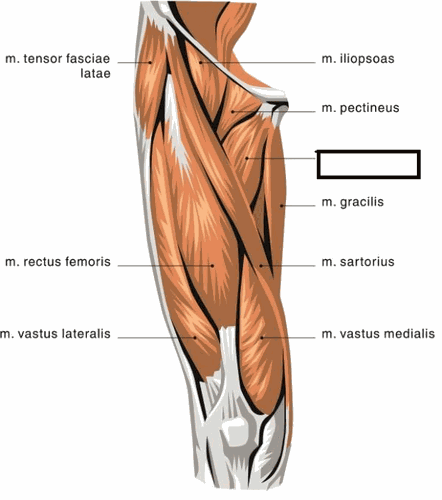
从图上可以看到,在正常情况下,大腿的肌纤维轮廓分明,这种时候无论是走路、跑步,甚至负重都没有问题。试想一下,当这种肌肉萎缩掉二分之一或三分之二时,还能支撑我们正常人的体重吗?我们还能行走自如?都不可能。
如果能够通过抗炎症的方式克服或延续肌肉萎缩和骨质疏松,试问:我们还需要拄拐杖和坐轮椅吗?答案显然是否定的!
慢性炎症的预防
一方面,慢性炎症几乎与所有慢性疾病有关,而引起炎症的原因又错综复杂,如代谢性内毒素血症,肥胖,氧化应激,机体的代谢产物(尿酸等),环境因素(环境中的内毒素)等等,慢性炎症的预防和治疗肯定不是一件轻而易举的事情。
另一方面,可以通过对慢性炎症的控制,达到预防和治疗与之相关的疾病的目的。比如,可以通过阻止慢性炎症,减缓衰老以及延缓与年龄相关的疾病的发病时间,从而获得健康与长寿。
1、补充益生菌
革兰氏阳性的双歧杆菌与内毒素血症呈负相关,增加肠道中双歧杆菌的数量能降低外周血中内毒素的表达水平。益生菌能改善糖耐量并恢复葡萄糖诱导的胰岛素分泌。另外,内毒素血症与葡萄糖耐受不良、空腹高胰岛素血症、炎症标记物、脂肪组织和体重增加等均成正相关,而双歧杆菌则与这些标记物呈负相关。因此,补充益生菌对减轻炎症是有益的。
补充益生菌较好的方式是自制酸奶加菊粉。
2、微量饮酒
众所周知,饮酒与高尿酸血症强烈相关,这可能与尿酸产出升高及排泄减少有关。同时,也有研究表明,少量饮酒可降低2型糖尿病的危险性,并降低胰岛素抵抗,冠心病,自主性甲状腺功能减退,骨质疏松,缺血性中风,健康状态等等。
3、关于西药抗慢性炎症
白介素1是引发局部及系统性炎症反应的细胞因子,它在心血管疾病的发病中起重要作用。因此,国外有人用一种全人源性抗IL-1β单克隆抗体预防该病的发生,其基本原理就是企图截断炎症反应的链条。问题是,几乎所有的炎症反应都不是单一的炎症因子作用的结果。因此,几乎所有这样的预防和治疗模式都失败了。这也充分暴露出西医在这个问题上的局限性。
同样,阿司匹林对C-反应蛋白升高者也具有预防心脑血管疾病,包括心肌梗死、中风、心源性猝死和周围血管疾病等的作用,但是,它也不能直接降低C-反应蛋白的表达水平。同时它的毒副作用,如消化道溃疡等也是被大家诟病的。
也有人将他汀类药物用于炎症的干预,但效果都极为有限。同时,鉴于有些他汀类药物可能会增加糖尿病以及认知障碍的危险,因此,确实需要其他抗炎症药物用以取代此类药物。
目前为止,用于预防慢性炎症的药物只有阿司匹林与他汀类。有人建议用所谓的免疫抑制剂抗炎症治疗,如甲氨蝶呤,这就有点黔驴技穷的味道了。须知这个药物是用来治疗恶性肿瘤的,毒副作用大尚且不说,其本身就可以诱导新的癌症的发生。
4、关于中药抗慢性炎症
如此看来,在抗慢性炎症这一问题上,医界似乎是一筹莫展了。其实不然,中药的天然属性及其多靶点协同作用几乎是对抗慢性炎症的必然选择,实践已证明了这一点。
我们将历时三十余年的中药研发成果投产并已面市。因此,可以大胆地预言,未来的一段时期,起码在抗慢性炎症这一领域,将是中药独领风骚的时代。
5、好的生活习惯:
饮食均衡保证充足睡眠
适量锻炼身体
避免烟草
每天一小口纯中药配制酒
每天200毫升自制酸奶加菊粉
。。。
参考文献:
1、Sikora, E. , Giovanni, S. , & Mario, B. . (2010). Curcumin, inflammation, ageing and age-related diseases. Immunity & Ageing I & A, 7(1), 1-1.
2、Cani, P. D. , Neyrinck, A. M. , Fava, F. , Knauf, C. , Burcelin, R. G. , & Tuohy, K. M. , et al. (2007). Selective increases of bifidobacteria in gut microflora improve high-fat-diet-induced diabetes in mice through a mechanism associated with endotoxaemia. Diabetologia, 50(11), 2374-2383.
3、Baliunas D. O., Taylor B. J., Irving H., Roerecke M., Patra J.,Mohapatra S. et al. Alcohol as a risk factor for type 2 diabetes: a systematic review and meta-analysis. Diabetes Care 2009; 32: 2123–32.
4、Baliunas D. O., Taylor B. J., Irving H., Roerecke M., Patra J.,Mohapatra S. et al. Alcohol as a risk factor for type 2 diabetes: a systematic review and meta-analysis. Diabetes Care 2009; 32: 2123–32.
5、Ronksley P. E., Brien S. E., Turner B. J., Mukamal K. J., Ghali W. A. Association of alcohol consumption with selected cardiovascular disease outcomes: a systematic review and meta-analysis. BMJ 2011; 342: d671.
6、Carle A., Pedersen I. B., Knudsen N., Perrild H., Ovesen L.,Rasmussen L. et al. Moderate alcohol consumption may protect against overt autoimmune hypothyroidism—a population-based case–control study. Eur J Endocrinol 2012; 167: 483–90.
7、Rapuri P. B., Gallagher J. C., Balhorn K. E., Ryschon K. L.Alcohol intake and bone metabolism in elderly women. Am J Clin Nutr 2000; 72: 1206–13.
8、Patra J., Taylor B., Irving H., Roerecke M., Baliunas D., Mohapatra S. et al. Alcohol consumption and the risk of morbidity and mortality for different stroke types—a systematic review and meta-analysis. BMC Public Health 2010; 10: 258.
9、Powers J. R., Young A. F. Longitudinal analysis of alcohol consumption and health of middle-aged women in Australia. Addiction 2008; 103: 424–32.
10、Ridker, P. M. , Thuren, T. , Zalewski, A. , & Libby, P. . (2011). Interleukin-1β inhibition and the prevention of recurrent cardiovascular events: rationale and design of the canakinumab anti-inflammatory thrombosis outcomes study (cantos). American Heart Journal, 162(4), 0-605.
11、Ridker, & P., M. . (2001). High-sensitivity c-reactive protein : potential adjunct for
12、global risk assessment in the primary prevention of cardiovascular disease. Circulation, 103(13), 1813-1818.
13、Sattar, N. , Preiss, D. D. , Murray, H. M. , Welsh, P. , & Ford, I. . (2010). Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. The Lancet,375(9716), 735-742.
14、Moreira, D.M.,da Silva, R.L.,Vieira, J.L.,et al.(2015).Inflammation and anti-inflammatory drugs in coronary artery disease.Am J Cardiovasc Drugs,,15(1):1-11.